2-デオキシ-D-グルコースの抗がん作用
【カロリー制限と類似の作用を示す2-デオキシ-D-グルコース】
カロリー制限による寿命延長の研究を行っている米国国立老化研究所(National Institute on Aging)のジョージ・ロス(George Roth)博士の研究グループは、カロリー制限と同じ効果を真似る薬の開発において、2-デオキシ-D-グルコース(2-Deoxy-D-glucose:以下2-DG)の可能性を研究していました。カロリー制限と同じ効果(抗老化や寿命延長効果)を示す薬をCalorie restriction mimetics (CRM:カロリー制限模倣化合物)と言います。 CRMには抗糖尿病薬のメトホルミン、赤ワインに含まれるレスベラトロール、ポリアミンの一種のスペルミジンなども知られていますが、2-DGはCRMとして最初に研究された物質です。現在でも抗老化の観点からの研究が行われています。
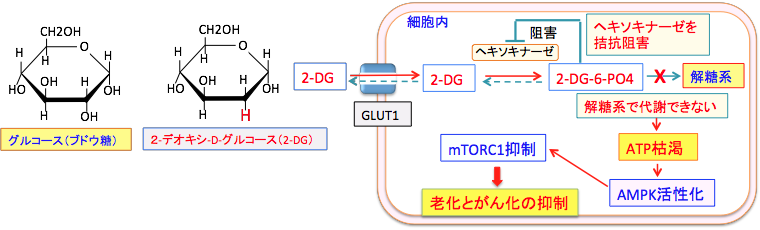
2-DGは、グルコース(ブドウ糖)の2位の水酸基(OH)が水素原子(H)に置換された物質(グルコース誘導体)です。 2-DGはグルコース(ブドウ糖)と同じグルコース輸送担体(グルコース・トランスポーター:GLUT)を利用して細胞内に取り込まれ、解糖系の最初のステップのヘキソキナーゼによって2-DG-6リン酸に変換されます。 リン酸化されて2-DG-6リン酸になるとGLUTを通過できなくなり、2-DG-6リン酸はその次の解糖系酵素では代謝できないため細胞内で蓄積します。 蓄積した2-DG-6リン酸はヘキソキナーゼをフィードバック阻害するので、正常のグルコースの代謝も阻害されます。グルコース代謝が阻害されてATP量が減少するとAMP活性化プロテイン・キナーゼ(AMPK)が活性化され、活性化されたAMPK はmTORC1(哺乳類ラパマイシン標的タンパク質)を抑制します。mTORC1は老化と発がん過程の両方を促進する働きがあるので、mTORC1の抑制は抗老化と抗がんの両方の効果になります。(下図) 。
2-デオキシ-D-グルコース(2-DG)はグルコースと同様に細胞内に取り込まれ、ヘキソキナーゼで2-DG-6-リン酸(2-DG-6-PO4)に変換されるが、それから先の解糖系酵素で代謝できないので、2-DG-6-PO4でストップしてATP産生ができない。蓄積した2-DG-6-PO4はヘキソキナーゼをフィードバック阻害するので、正常なグルコースの解糖系での代謝も阻害される。その結果、細胞内のATPが減少し、AMP活性化プロテイン・キナーゼ(AMPK)が活性化される。活性化したAMPKはmTORC1(哺乳類ラパマイシン標的タンパク質)を抑制するので、細胞の老化とがん化を抑制することになる。
普通に食事を摂取しても2-DGによってグルコースの代謝を抑制すれば、たくさん食べても太らずにすむし、カロリー制限と同じメカニズムで老化予防に有効ではないかというのが、2-DGの抗老化作用のメカニズムです。
線虫の実験では、2-DGが寿命を顕著に延長する結果が得られています。 しかし、ラットの実験では2-DGを大量に長期間投与すると心筋細胞の空砲化と死亡率の上昇などの毒性が確認されています。(Toxicol Appl Pharmacol 243(3): 332-9, 2010年) つまり、動物にとっては老化予防や寿命延長の目的では2−DGは現実的とは言えないようです。 ただし、てんかんやがんの治療目的においては、臨床効果の方が毒性より上回っていると考えられ、人間での臨床試験が行われています。
また、適量を使用すれば、毒性が出ずに抗老化作用や健康作用が期待できる可能性は残されています。最近も2-DGの抗老化作用に関する研究は幾つも報告されています。 例えば、2-デオキシ-D-グルコースがケトン体の産生を高めて神経細胞におけるミトコンドリアでのエネルギー産生を高めることによってアルツハイマー病を改善する作用が動物実験で確認されています。(PLos ONE 6(7): e21788, 2011年)
アルツハイマー病が発症する前に神経細胞のミトコンドリアでのエネルギー産生が低下することが報告されており、2-DGはケトン体の産生を増やすことが知られています。この論文では、マウスのアルツハイマー病の実験モデルに2-DGを投与すると、神経細胞のミトコンドリアでのエネルギー産生が増え、ベータアミロイドの沈着などアルツハイマー病の病変が軽減することが報告されています。カロリー制限やケトン食がアルツハイマー病の治療に有効であることは多くの研究で指示されています。2-DGはカロリー制限と同様な作用を示し、ケトン体の産生を増やす点で抗老化作用が期待されています。 このように解糖系でのグルコースの代謝を2−DGで抑制するとカロリー制限と同じように抗老化作用が期待できます。さらに、2-DGはがん細胞の増殖を抑制する作用があります。
【グルコースの取込みが多いがん細胞は増殖活性が高い】
一般的にグルコースの取込みの多いがん細胞ほど増殖が早く、悪性度が高く、予後が悪いと言えます。取り込まれたグルコースがエネルギー産生と細胞を構成する成分の合成に使われるからで、グルコースの取込みが多いことは増殖活性が高いことを意味します。 したがって、がん細胞におけるグルコースの取込みや解糖系での代謝を阻害すると、がん細胞の増殖活性を低下させることができます。
また、抗がん剤治療や放射線治療にグルコースの取込みや解糖系を阻害する治療を併用すると、抗がん剤や放射線治療の効き目を高めることができます。 がん細胞が抗がん剤や放射線でダメージを受けても、エネルギー(=ATP)と細胞成分を作る材料、すなわちグルコースが十分に供給されておれば、ダメージを修復して増殖を続けることができます。しかし、がん細胞におけるグルコースの取込みや利用を阻害すれば、ダメージを修復することができません。
グルコースの取込みやエネルギー産生過程を阻害する方法は、抗がん剤や放射線に対するがん細胞の感受性を高める効果が期待でき、がん治療の重要なターゲットになっています。(下図)
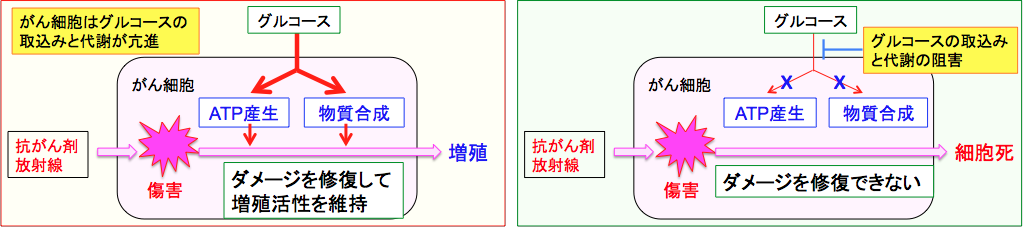
(左)がん細胞はグルコーストランスポーター1(GLUT1)の発現量が多く、グルコースの取込みと代謝(解糖系とペントース・リン酸経路)が亢進してATP産生と細胞を構成する物質(細胞膜や核酸など)の合成が亢進している。抗がん剤や放射線照射によって細胞がダメージを受けても、グルコースの取込みと代謝の亢進によって、ダメージを修復して増殖活性を維持できる。
(右)グルコースの取込みや代謝が阻害されると、ダメージの修復に必要なATPも物質合成も行えなくなる。そうなると抗がん剤や放射線で受けたダメージを修復できないので、細胞死をきたすことになる。。
【2-DGで解糖系を阻害するとがん細胞は死滅する】
2-DGはグルコース(ブドウ糖)と同じグルコース輸送担体(グルコース・トランスポーター)のGLUT1を利用して細胞内に取り込まれ、解糖系の最初のステップのヘキソキナーゼによって2-DG-6リン酸に変換されます。 リン酸化されて2-DG-6リン酸になるとGLUT1を通過できなくなり、2-DG-6リン酸はその次の解糖系酵素では代謝できないため細胞内でどんどん蓄積します。
がん細胞内に蓄積した2-DG-6リン酸はヘキソキナーゼを阻害するので、通常のグルコースの代謝も阻害されます。 2-DGを取り込んでエネルギー産生が低下するとそのストレス応答によってグルコーストランスポーター(GLUT1)の発現がさらに増え、2-DGの取り込みをさらに増やすことになります。 したがって、がん細胞には正常細胞に比べてより多くの2-DGが取込まれ、エネルギー産生と物質合成の阻害による影響はがん細胞で大きくなります。 つまり、糖質制限やケトン食のときに2-DGを併用すると、2-DGが優先的にがん細胞に取り込まれ、解糖系やペントース・リン酸経路を阻害して、がん細胞を内部から崩壊させることができるのです。
2-DGががん細胞の増殖を抑制する効果が指摘されたのは1950年代です。「細胞のエネルギー源であるグルコースの誘導体を取り込ませれば、がん細胞の増殖を抑制できる」というアイデアは、もう60年も前に研究されており、グルコースの誘導体の抗腫瘍活性が検討され、2-DGに強い抗腫瘍効果があることが証明されています。 しかし、2-DGを使ったがん治療は、その後あまり注目されなかったようです。その理由の一つは、がんの治療においては、「強い毒性をもった化合物を使ってがん細胞を一掃するような治療法」が1950年代以降は主流になっていたからだと思われます。 そのため、「エネルギー産生経路を阻害してがん細胞の増殖を低下させる」というようなアイデアは注目されなかったのかもしれません。
しかし、がん細胞のエネルギー産生の特徴であるワールブルグ効果が再評価されるようになり、がん細胞のエネルギー産生と物質合成を阻害する方法として、2-DGにも注目が集まるようになり、多くの動物実験で抗腫瘍効果が証明され、人間での臨床試験も実施されるようになったということです。
【2-DGは正常細胞を抗がん剤や放射線のダメージから保護する】
2-デオキシ-D-グルコース(2-DG)はがん細胞の解糖系を阻害するので、がん細胞の増殖速度を低下させる効果があります。がん細胞のエネルギー産生や物質合成の経路を阻害すると、抗がん剤や放射線に対するがん細胞の感受性が高まります。 2-デオキシ-D-グルコース(2-DG)は抗がん剤や放射線に対するがん細胞の感受性を高めるだけでなく、抗がん剤や放射線による正常細胞のダメージを軽減する効果があるという報告があります。
がん細胞は正常細胞に比べてグルコース(ブドウ糖)の取込みが多く、ATP産生や細胞分裂するための物質合成に大量のグルコースを必要としています。したがって、グルコースの取込みや利用を妨げれば、ATP産生や物質合成が低下し、抗がん剤や放射線治療の効き目が高くなります。 がん細胞はグルコーストランスポーターを多く発現しているので、2-DGの取込みも多く、2-DGによるグルコース代謝の阻害作用が著明に現れます。培養細胞を使った実験や動物にがん細胞を移植した動物実験で、2-DGを投与すると抗がん剤や放射線治療の治療効果が高まることが多くの実験系で確認されています。
さらに動物実験で、2-DGが脳や心臓に対する抗がん剤や放射線のダメージを軽減する作用が認められています。その作用機序についてはまだ十分に解明されていませんが、AMP活性化プロテインキナーゼ(AMPK)の活性化など複数のメカニズムが示唆されています。
このように、2-DGはがん細胞の抗がん剤感受性や放射線感受性を高め、正常細胞に対しては抗がん剤や放射線のダメージから守る作用があります。 また、抗がん剤や放射線治療に2-DGを併用すると抗腫瘍免疫を誘導できることが報告されています。 がんや感染症に対する免疫応答で重要な記憶キラーT細胞(memory CD8+T cell)の働きを高めるという報告もあります。
以上のように、2-DGは様々なメカニズムで抗腫瘍作用を示し、特に抗がん剤や放射線治療との併用で、抗腫瘍効果を高めるだけでなく、正常細胞を保護する作用もあるので、がん治療の補完として利用価値は高いと言えます。適切な量を使用すれば抗老化にも有効かもしれません。
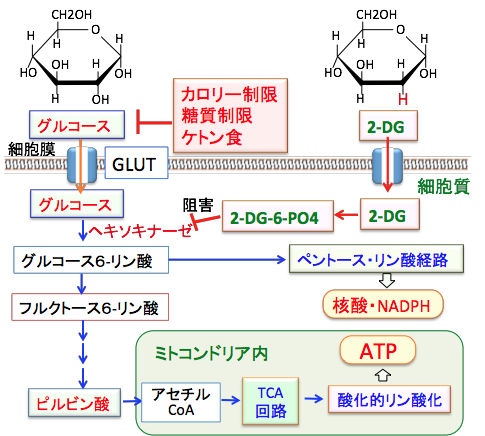
2−デオキシ-D-グルコース(2-DG)はグルコースと同じようにグルコーストランスポーター(GLUT)を通って細胞内に入る。グルコースはヘキソキナーゼでグルコース-6-リン酸に変換されてさらに解糖系酵素で分解されてATP産生へ使われ、ペントースリン酸回路で核酸やNADPHの合成に利用される。2−DGはヘキソキナーゼで2-デオキシ-D-グルコース-6-リン酸(2-DG-6-PO4)に変換されるが、2-DG-6-PO4はその先の解糖系酵素で代謝できない。細胞質内で蓄積した2-DG-6-PO4はヘキソキナーゼをフィードバック阻害するので、解糖系でのグルコース代謝が阻害されてATP産生や核酸やNADPHの産生が低下する。
2-デオキシ-D-グルコースの1ヶ月分の費用の目安は20,000円〜50,000円です。
糖質制限を行っていない場合は1日服用量は体重1kg当たり30〜60mgです。体重50kgの場合で1日に1.5g〜3gを服用します。(1ヶ月に45g〜90g)
糖質制限やケトン食を行っている場合は1日服用量は体重1kg当たり20〜30mgです。体重50kgの場合で1日に1〜1.5gの服用になります。(1ヶ月に30g〜45g)
50gが30,000円で処方しています。2-DGに加えて、メトホルミンとラパマイシンを併用すると抗腫瘍効果を高めることができます。(詳しくはこちらへ)