メトロノミック・ケモテラピー(Metronomic Chemotherapy)
【最大耐用量を投与する標準治療】
最初の抗がん剤はナイトロジェンマスタードで、第一次世界大戦に化学兵器として使われたマスタードガスのイオウ原子を窒素に置き換えた化合物です。DNAをアルキル化することによって核酸の合成を阻害して細胞の増殖を抑えます。
ナイトロジェンマスタードが最初にがん患者に使用されたのは1946年で、非ホジキンリンパ腫の症例で劇的な効果が認められました。 その後毒性を弱めたナイトロジェンマスタード誘導体が開発され、シクロフォスファミドやメルファランといった抗がん剤が現在も使用されています。これらはアルキル化剤という抗がん剤に分類されています。通常の抗がん剤治療は、副作用が耐えられる最大量(最大耐用量)を投与してがん細胞を短期間で死滅させる方法が基本になっています。 抗がん剤に対する耐性が出てくる前に短期間にがん細胞を全滅させる方が良いと考えるからです。白血病や悪性リンパ腫ではこの方法が有効です。
しかし、固形がんの場合は、この方法は必ずしも有効ではありません。 精巣腫瘍や小細胞性肺がんのように抗がん剤治療が著効を示す固形がんもありますが、多くの固形がん(肺がんや膵臓がんや胃がんなど)に対しては、抗がん剤の効き目は極めて限定的です。 固形がんの多くは抗がん剤治療に抵抗性を示し、抗がん剤治療だけでは全身に広がったがん細胞を根絶させることは、ほぼ不可能です。抗がん剤の投与量を増やせば増やすほど、がん細胞を死滅させる効果は強くなります。しかし一方、抗がん剤の投与量が増えれば増えるほど正常細胞のダメージによる副作用が強くなり、投与量が限界を超えれば患者さん自身が死亡してしまいます。
患者さんが副作用に耐えられる投与量の範囲で最大限の投与量を設定するのが、最も効果が高いという意見が一般的ですが、この最大耐用量の抗がん剤投与の方法には様々なデメリットと欠陥が指摘されています。
正常組織にダメージを与えて強い副作用を引き起こすだけでなく、免疫力を低下させたり、がん組織の血管新生を促進する可能性や、抗がん剤耐性のがん細胞の出現を促進する可能性などが指摘されています。
【低用量の抗がん剤を継続的に服用するメトロノミック・ケモテラピー】
最大耐用量を投与する標準的な抗がん剤治療に代わって、最近注目を集めているのが、低用量頻回投与の抗がん剤治療で、メトロノミック・ケモテラピー(Metronomic Chemotherapy)と呼ばれる治療法です。
メトロノミックとは、リズムを刻む「メトロノームの様な」という意味で、メトロノミック・ケモテラピーとは、メトロノームのように規則的に低用量の抗がん剤を頻回に投与していく抗がん剤治療法です。
最大耐用量を投与する抗がん剤治療では、正常組織のダメージを回復させる期間をもうけるために、週一回とか月に一回というように間歇的な投与法になりますが、この休薬期間に腫瘍血管内皮細胞が急速に再生し、腫瘍血管の新生が亢進して、腫瘍の増大が起こります。
一方、メトロノミック・ケモテラピー(休薬期間をもうけない長期間の低用量投与)では、腫瘍の増大に必要な血管新生を抑制でき、がん細胞の増殖を阻止できると考えられています。 さらに、低用量の投与であるため、副作用が少なく、また免疫細胞の働きを抑えている制御性T細胞の働きを阻害するので、免疫力はむしろ高くなるという効果も報告されています。(下図)
近年、メトロノミック・ケモテラピーの有効性を示す報告が多くなっており、最大耐用量を投与する現行の抗がん剤治療に代わる「体にやさしい抗がん剤治療法」として注目されつつあります。
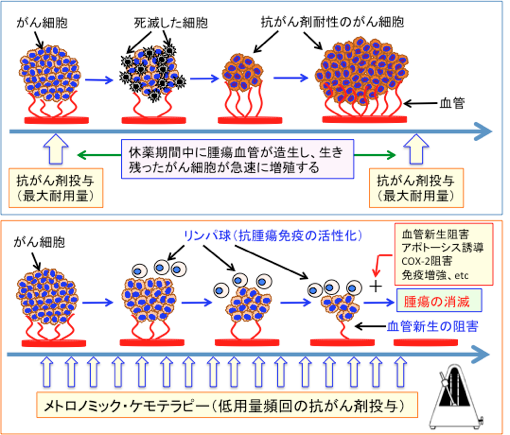
図:通常の抗がん剤治療は、副作用に耐えられる最大量(最大耐用量)の抗がん剤を投与する。この場合、正常組織へのダメージも強いので副作用も強く現れる。また、正常組織のダメージを回復させる必要があるため、抗がん剤投与の間に休薬期間が必要であるが、この休薬期間に腫瘍血管が急速に再生し、生き残ったがん細胞が増殖する。抗がん剤が効きにくい強いがん細胞が選択的に生き残るので、がん組織は次第に抗がん剤が効きにくい細胞が多くなってくる。(図の上)
一方、休薬期間を設けないで、メトロノームのように定期的に頻回に低用量の抗がん剤を投与するメトロノミック・ケモテラピー(Metronomic Chemotherapy)では、血管新生が抑制されて抗腫瘍効果を発揮する。また、低用量の抗がん剤投与は副作用が少なく、免疫系組織の抑制も回避できる。低用量の抗がん剤投与は腫瘍免疫を抑制する制御性T細胞の活性を阻害する作用があり、その結果、がん細胞を排除する抗腫瘍免疫が増強される。メトロノミック・ケモテラピーだけでは抗腫瘍効果に限界があるが、血管新生阻害やアポトーシス誘導やシクロオキシゲナーゼ-2(COX-2)阻害や免疫増強などの治療法を併用すると、さらに抗腫瘍効果を高め、腫瘍を消滅させることも可能になる(下図)。
【高用量の抗がん剤投与は腫瘍血管の新生を促進する】
最大耐用量の抗がん剤投与の問題点の一つは、最大耐用量の抗がん剤投与によってダメージを受けた正常組織の回復を計るために休薬期間が必要な点です。そして、この休薬期間にがん組織を養う腫瘍血管の新生が促進されて、腫瘍の増大が起こります。 以下のような論文があります。
がん組織の増殖には血管発生(vasculogenesis:血管内皮前駆細胞による新しい血管の形成)が必要であることを示すエビデンスが増えている。 この論文では、ヒト悪性リンパ腫細胞を移植した免疫不全マウスを用いた動物実験モデルにおいて、シクロフォスファミドを21日間の休薬期間をもうける最大耐用量投与の場合と、低用量で継続的に頻回投与するメトロノミックなスケジュールで投与する場合で、血中に循環する血管内皮前駆細胞の移動と生存に対して逆の作用を示すことを明らかにした。
最大耐用量のシクロフォスファミドを投与されたマウスでは、シクロフォスファミド投与終了して数日後には大量の血管内皮前駆細胞が血中に出現し、腫瘍は急速に薬剤耐性になった。 一方、シクロフォスファミドの低用量頻回投与を受けたマウスでは、血中の血管内皮前駆細胞の数と生存率は継続的に減少を示し、腫瘍組織の増大が持続的に抑制された。
これらの結果は、抗がん剤のメトロノミックな低用量頻回投与法は骨髄から血中への血管内皮前駆細胞の移動を阻止することによって、新しい血管の形成(血管発生)による腫瘍の増大を抑制することを示しており、有用な治療法となりうる可能性がある。血管内皮前駆細胞(endothelial progenitor cells)というのは、骨髄由来の血液中に存在する幹細胞で、がんや創傷治癒や虚血部位において血管形成に関与する細胞です。サイトカインや成長因子などの作用で骨髄から動員されて新たな血管形成(血管発生)に使われます。
従来、成体の血管形成は、既存血管の内皮細胞が増殖・遊走して新たな血管を作り出す血管新生(angiogenesis)という概念が中心でしたが、1997年に成人末梢血液中に血管内皮前駆細胞(Endothelial Progenitor Cell: EPC)が発見されてから、胎生期のみに起こるとされていた血管発生(vasculogenesis)という現象が成体においても認められ、局所でEPCが増殖・分化して血管新生に関わっていることが明らかになっています。
通常、EPCは骨髄に存在していますが、ケガなどで組織や血管が損傷されるとEPCが血液の中を流れて、損傷部位に呼び集められ、新たな血管を作り、組織の修復を行います。
再生医学では虚血性疾患(閉塞性動脈硬化症や糖尿病性足壊疽など)の治療への利用が研究されています。
一方、がん治療においては、この論文にあるように、腫瘍血管の形成に関与し、腫瘍の増大を引き起こす原因としてEPCが検討されています。
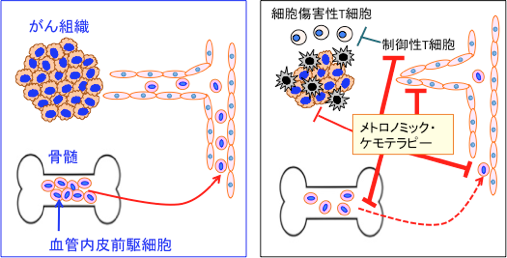
がん組織が大量の抗がん剤で死滅すると、正常組織の修復と同じ機序で、がん組織の血管を修復・再生するためにEPCが骨髄から動員され、腫瘍血管の形成と増生に利用されるのです。 骨髄からのEPCの動員や血中のEPCの数を減らすことががん治療に有効だと考えられています。 通常の最大耐用量を投与する抗がん剤治療では、正常組織のダメージを回復するために設けた休薬期間にEPCの動員が起こり、腫瘍血管の新生が亢進し、その結果、腫瘍の増大が促進されるという現象が起こります。 一方、抗がん剤の低用量頻回投与によるメトロノミック・ケモテラピーではEPCの動員が起こらず、血中のEPCの数も減少するので、腫瘍の増大が起こらないという結果です(下図)。
図:がん組織を養う腫瘍血管は、既存血管の内皮細胞が増殖・遊走して新たな血管を作り出す血管新生(angiogenesis)の他に、骨髄に存在する血管内皮前駆細胞(endothelial progenitor cells)という幹細胞が骨髄から動員されて血管形成に関わっている。高用量の抗がん剤投与では、血管内皮前駆細胞が骨髄から動員されて休薬期間中に血管の増生が促進される。一方、低用量の頻回に投与するメトロノミック・ケモテラピー(Metronomic Chemotherapy)では、血管内皮前駆細胞の骨髄からの動員が阻止され、血中の血管内皮前駆細胞は死滅し、血管形成が阻止される。さらにがん細胞に対する直接的な抗腫瘍作用や、制御性T細胞の阻害による抗腫瘍免疫の活性化なども指摘されている。これらの相乗効果によってがん細胞の増殖を抑制する。
また、高用量の抗がん剤によってがん組織が強くダメージを受けると、細胞の遊走性や増殖を促進するケモカインの分泌やがん細胞におけるケモカイン受容体の発現の亢進が起こって、がん細胞の浸潤や転移が促進されることが報告されています。
つまり、強い抗がん剤治療は、それでがんが全滅できなければ、最終的にはがんをより悪化させることにつながるのです。
強い抗がん剤治療で一時的にもがんが縮小すると患者さんも医師も安心しますが、長期的にはあまり良い結果は得られないのです。
【がん組織には多くの正常細胞が存在する】
20世紀末までのがん研究では、「がんとは細胞の病気」という考えで研究を行われていました。つまり、がん細胞で起こっているシグナル伝達系や遺伝子の異常の解明ががん研究の主体になっていました。そして、がん治療もがん細胞だけをターゲットに考えていました。
しかし、がん研究はがん細胞だけをターゲットにすればいいという単純なものではありません。がん細胞が増殖するためには、がん細胞の自律増殖能だけでは不十分です。 がん組織は、正常組織から血管や間質細胞を取込み、がん細胞の生存と増殖に有利な特殊な微小環境を形成しています。 がん組織のうち30から99%が正常細胞と言われています。がん細胞の塊のように思えても、がん細胞を養う血管や増殖の基盤になる結合組織を作る線維芽細胞が必要です。
がん組織の中にはがん細胞は数%しか占めていない場合もあります。 がん組織中の正常細胞が、結合組織や細胞外マトリックス、増殖因子、サイトカイン、血管網を提供し、がん細胞の増殖や転移を支配しています。
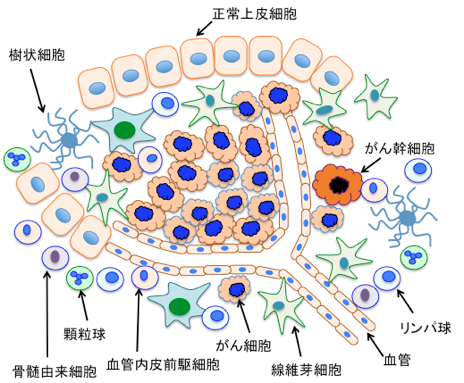
つまり、腫瘍というのは、「増殖異常を来したがん細胞の単なる集まり」ではなく、「がん細胞とその周囲に集まった正常細胞(腫瘍微小環境)から構成された制御を失った組織」であり、腫瘍微小環境(tumor microenvironment)ががん組織の進行性の増大をサポートしているのです。(下図) メトロノミックテラピーはがん細胞ではなく、この間質を主なターゲットにする治療とも言えます。
図:がん組織はがん細胞と様々な正常細胞から構成されており、がん細胞の増殖や転移は、がん細胞と正常細胞の相互作用によって決められる。がん細胞自身をターゲットにする治療の他に、血管新生の阻害、免疫細胞の活性化、結合組織によるがん細胞の封じ込めなど、正常細胞をターゲットにした様々な治療法を併用することによってがんの治療効果を高めることができる。(参考:Transl Cancer Res. 2013 August 1; 2(4): 309–319のFig1)
【メトロノミック・ケモテラピーの効果を高める併用療法】
メトロノミック・ケモテラピーは抗がん剤の1回の投与量を少なくして、頻回に投与する抗がん剤治療です。経口の抗がん剤を通常より少ない量で毎日服用するような治療法です。 副作用は少なく、腫瘍血管の増生阻害や抗腫瘍免疫の活性化などによってがん組織の増大を阻止し、長期的ながん縮小あるいはがんとの共存を目指す治療法です。
低用量の抗がん剤を使った方法以外にも、抗がん生薬を多く使った漢方治療も同様の効果が期待できます。
これらの治療法にさらに、血管新生阻害作用、アポトーシス誘導作用、分化誘導作用、免疫増強作用などをもった治療法を組み合わせれば、さらに抗腫瘍効果を高めることができます。次のような論文があります。
【要旨】
研究の背景:再発を繰り返す治療抵抗性の悪性腫瘍の小児患者の予後は極めて不良であり、新規で有効な治療法の開発が望まれている。有望な治療法の一つがメトロノミック化学療法(metronomic chemotherapy)である。欧州の小児疾患センターの3施設において進行した固形がんの小児患者74例を対象に行ったメトロノミック化学療法の結果を報告する。
方法:COMBAT療法はCombined Oral Metronomic Biodifferentiating Antiangiogenic Treatment(がん細胞の分化誘導作用と血管新生阻害作用のある薬剤を組み合わせた低用量頻回投与療法)の略で、テモゾロマイド(temozolomide)、エトポシド(エトポシド)、セレコキシブ(celecoxib)、ビタミンD、フェノフィブラート(fenofibrate)、レチノイン酸(retinoic acid)を組み合わせた治療法で、それぞれ低用量で毎日投与を行う治療法である。患者は2004年から2010年の間に募集した。
結果:2年生存率は43.1%であり、生存期間の中央値は15.4ヶ月(1.3~69.9ヶ月)であった。74例のうち50例(68%)は死亡し、24例は生存している。この24例のうち6例(8%)は病状が進行しており(progressive disease)、7例(9%)は病状安定か部分奏功(stable disease/partial response)であり、11例(15%)は完全奏功(complete response)であった。奏功するまでの平均期間は6ヶ月であった。 治療開始前にX線検査で腫瘍の大きさを測定できた62例のうち25例(40%)で、腫瘍縮小や病状安定の所見を認めた。この25例中14例では6ヶ月以内に臨床的な改善を認めた。 副作用は軽度で外来通院にて治療が可能であった。グレード2以上の非血液的毒性の発症に関しては、グレード3の肝障害を8例に認め、グレード3の口唇炎が16例に認められた。
結論:COMBAT療法は再発性/治療抵抗性の悪性腫瘍の小児患者に対して、毒性が低く、十分に実施可能で有効な治療法である。この研究では、メトロノミック・ケモテラピー(低用量のテモゾロマイド、エトポシド)にシクロオキシゲナーゼ-2阻害剤のセレコキシブ、分化誘導剤のビタミンD、レチノイン酸、フェノフィブラートを併用しています。 ビタミンDとレチノイン酸とフェノフィブラートは核内受容体を介して細胞分化を誘導する組合せです。セレコキシブ(商品目:セレコックス)はCOX-2阻害作用によってがん細胞の増殖を抑え、抗腫瘍免疫を活性化する作用があります。
がん治療においてメトロノミック・ケモテラピーの理論と方法論は役にたちます。メトロノミック・ケモテラピーに関するご質問やご相談はメール(info@f-gtc.or.jp)か電話(03-5550-3552)でご連絡ください。