トル様受容体7のリガンド(イミキモド)を使用した抗腫瘍免疫増強法
がんの治療法には、抗がん剤や放射線治療のようにがん細胞を直接死滅させることを目標にする方法と、体に備わった免疫システムを活性化してがん細胞を免疫的に排除する方法(免疫療法)があります。
免疫療法には様々な方法があります。最近の研究で、がん細胞に対する獲得免疫を活性化するためには、樹状細胞の活性化など自然免疫を刺激することが必要であることが明らかになっています。
樹状細胞を活性化する方法として、トル様受容体7(Toll-like Receptor 7: TLR7)のリガンドであるイミキモド、インターロイキン-12(IL-12)の産生を高めて樹状細胞の成熟を促進するピドチモドの併用が有効です。
一方、がん組織では、T細胞などのエフェクター細胞の働きを抑制する様々な要因が存在します。例えば、がん細胞やマクロファージから産生されるシクロオキシゲナーゼ-2(COX-2)によって産生されるプロスタグランジンE2(PGE2)はがん細胞に対するT細胞の働きを抑制します。また、がん組織にはT細胞の働きを抑制する骨髄由来抑制細胞(MDSC)や制御性T細胞(Treg)が増えています。したがって、PGE2の産生を抑制する方法や、MDSCやTregの働きを阻害する方法はがん細胞に対する免疫的攻撃を増強できます。
COX-2阻害剤の celecoxib(商品名セレコックス) 、MDSCの働きを阻害するシメチジンやシクロフォスファミド、MDSCの分化を促進して免疫抑制活性を低下させるレチノイドとビタミンD3を併用すると、がん細胞に対する免疫細胞の働きを高めることができます。
さらに、T細胞の働きを高めるアジュバンド効果のある漢方薬の併用も、抗腫瘍効果を高めます。
これらの組合せによるがん細胞に対する免疫細胞の活性化の仕組みを下図にまとめています。
①イミキモドはトル様受容体TLR7を刺激して未熟樹状細胞の成熟・活性化を促進する。②ピドチモドは樹状細胞の成熟とIL-12産生を促進して1型ヘルパーT細胞(Th1)を増やし、ナチュラルキラー細胞(NK細胞)を活性化する。③プロスタグランジンE2(PGE2)はIL-12の産生を抑制して2型ヘルパーT細胞(Th2)への分化を誘導するので、COX-2阻害剤のCelecoxibはPGE2の産生を阻害してTh2への分化誘導を阻止する。④PGE2は骨髄由来抑制細胞(MDSC)の増殖を促進するので、CelecoxibはMDSCの増殖を阻止する。⑤漢方薬(紅参、黄耆、川芎など)はTh1サイトカインの産生を高めて細胞性免疫を活性化する。⑥シメチジンとシクロフォスファミドはMDSCの活性や生存を阻害する。⑦レチノイドとビタミンD3は未熟なMDSCを成熟させ分化誘導によって免疫抑制活性を低下させる。 1ヶ月分の費用の目安:
基本は、イミキモド+ピドチモド+セレコックス+シメチジンです。この組合せで1ヶ月分が4万円から5万円程度になります。進行がんなどで効果を高める必要があるときに、シクロフォスファミド、漢方薬、All-Trans レチノイン酸、ビタミンD3を追加します。
ご希望の方はメール(info@f-gtc.or.jp)でご連絡下さい。
【がん組織は免疫細胞の働きを抑制する微小環境を作っている】
樹状細胞ががん細胞の死骸を分解してがん抗原を提示すると、このがん抗原にぴったり結合する受容体を持ったナイーブヘルパーT細胞、ナイーブキラーT細胞、ナイーブB細胞が抗原特異的に活性化され、増殖します。ナイーブ細胞というのはまだ一度も抗原刺激を受けていない細胞のことです。
抗原特異的に活性化されて増殖したリンパ球は、それぞれの役割をはたすべき働きます。このような細胞をまとめて「エフェクター細胞(effector cell)」と呼びます。「エフェクター」とは「作用する」「効果を発揮する」という意味です。 つまり、がん細胞の攻撃のために実際に働く細胞のことです。
これらの免疫細胞の働きを高める治療法はがんの治療法として期待されています。しかし現実的には、多くの免疫療法はあまり効果が認められていません。
その大きな理由は、がん組織には免疫細胞の働きを抑制する様々な細胞やサイトカインや化学物質が増えていて、免疫細胞が十分にがん細胞を攻撃できないからです。 がん細胞を攻撃する目的で免疫担当細胞ががん組織に入っていっても十分な働きができないためです。 つまり、がん組織は免疫細胞の働きを抑制するような微小環境を自ら作り出しています。
例えば、がん組織にはマクロファージなどの炎症細胞から活性酸素やプロスタグランジンE2(PGE2)の産生が増えています。 PGE2と活性酸素は、免疫担当細胞(樹状細胞、リンパ球、NK細胞など)の働きを抑制します。 一方、PGE2は骨髄由来抑制細胞を動員しがん組織内で増えます。 骨髄由来抑制細胞(Myeloid-derived suppressor cells: MDSCs)は顆粒球のマーカーと単球/マクロファージのマーカーとを同時に発現している未熟な段階の骨髄由来細胞で、免疫反応を強力に抑制する働きを持っています。
骨髄由来抑制細胞はアルギナーゼや活性酸素、一酸化窒素、IL-10、TGF-βなどの産生を介して免疫担当細胞の活性を阻害したり、制御性T細胞(Treg)の誘導をきたすことによって免疫抑制作用を発揮します。制御性T細胞は免疫応答を抑制的に制御しているT細胞の一種です。
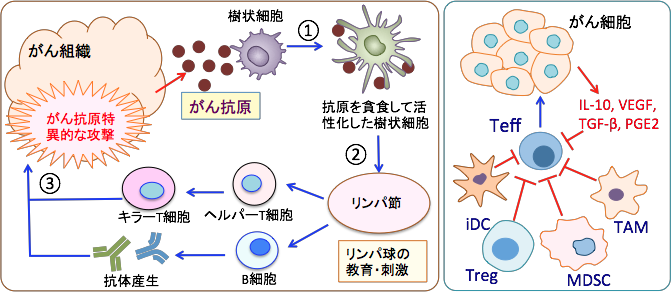
右図:①樹状細胞は死滅したがん細胞を取り込んで分解し、ペプチド(アミノ酸が数個から数十個つながったもの)をMHC(主要組織適合抗原複合体)分子の上に提示する。②抗原を提示している活性化した樹状細胞はリンパ節に移動する。③リンパ節内で樹状細胞が提示する抗原とぴったり結合する受容体をもつナイーブ細胞が活性化され、増殖する。がん抗原に特異的に反応するB細胞はがん抗原に対する抗体を産生し、ヘルパーT細胞はキラーT細胞(細胞傷害性T細胞)を活性化してがん細胞を攻撃する。これらがん細胞を攻撃するために働く細胞をエフェクター細胞という。
左図:がん組織の微小環境においては、様々な要因がエフェクターT細胞(Teff)の働きを抑制している。がん組織から産生されるIL-10、TGF-β、VEGF、プロスタグランジンE2(PGE2)は骨髄由来抑制細胞(MDSC)を動員し、樹状細胞の成熟を抑制し、エフェクター細胞(Teff)の機能を抑制している。さらに、がん組織には制御性T細胞(Treg)が増えており、Teffの機能を抑制し、IL-10の産生を亢進し、樹状細胞の成熟を抑制している。腫瘍関連マクロファージ(TAM)はTeffの機能を抑制する。未熟な樹状細胞(iDC)はTregの腫瘍内集積を亢進し、Teffの働きを抑制する。 このような複数のメカニズムでがん組織内では免疫担当細胞の働きは抑制され、がん細胞を排除できない環境になっている。
【がん細胞に特異的な獲得免疫が始動するには自然免疫の活性化が必要】
免疫システムは病原体やがん細胞から生体を守る働きを担っています。この免疫システムは自然免疫と獲得免疫に分けられます。
自然免疫は先天的に備わった免疫で、微生物などに特有の分子パターンを認識して異物を攻撃します。マクロファージや好中球には細菌などの病原体に共通した情報を認識できる受容体を細胞表面に持っていて、病原体を認識して貪食します。 さらにマクロファージはナチュラルキラー細胞を活性化します。 ナチュラルキラー(natural killer)細胞(略してNK細胞)は、ターゲットの細胞を殺すのにT細胞と異なり事前に感作させておく必要が無いことから、生まれつき(natural)の細胞傷害性細胞(killer cell)という意味で名付けられました。
「感作」というのは、前もって抗原に対する認識能を高めておくことで、感作させておく必要がないというのは、初めて出あった細胞でも、直ちにその異常細胞を認識して攻撃できるということです。 ナチュラルキラー細胞(NK細胞)は、MHCクラスI分子が喪失した細胞(自己性を喪失した異常な細胞)を認識して攻撃します。 NK細胞の細胞質にはパーフォリンやグランザイムといった細胞傷害性のタンパク質をもち、これらを放出してターゲットの細胞を死滅させます。 がん細胞を見つけると直ちに攻撃するため、がんに対する第一次防衛機構として、特に発がん過程の初期段階でのがん細胞の排除において重要な役割を果たしています。
一方、獲得免疫は,後天的に外来異物の刺激に応じて形成される免疫です。高度な抗原特異性と免疫記憶を特徴とします。 マクロファージや樹状細胞が、がん細胞からがん抗原ペプチドと呼ばれる小さな蛋白質を捕足し、その情報がヘルパーT細胞に伝えられ、その情報に従って特定のがん抗原に対する免疫応答が引き起こされるのが獲得免疫です。 キラーT細胞は、がん抗原で活性化されて初めて細胞傷害活性を持つようになります。すなわち、細胞傷害活性を持たないナイーブキラーT細胞(抗原刺激を一度も受けたことがないキラーT細胞)が抗原提示細胞から抗原ペプチド(がん抗原)を提示され、その抗原とぴったり結合するキラーT細胞が活性化されて増殖し、がん細胞に対して特異的な細胞傷害活性を持つ細胞傷害性T細胞(キラーT細胞)となり、がん細胞を攻撃するようになります。
細胞傷害性T細胞(CTL)は細胞傷害物質であるパーフォリン、 グランザイム, TNF(tumor necrosis factor)などを放出したり、ターゲット細胞のFasを刺激してアポトーシスに陥らせることでがん細胞やウイルス感染細胞を死滅させます。
細胞傷害性T細胞の一部はメモリーT細胞となって、異物に対する細胞傷害活性を持ったまま宿主内に記憶され、次に同じ異物(抗原)に暴露された場合に対応できるよう備えます。
「自然免疫」は、マクロファージや好中球などの食細胞が侵入した病原体やがん細胞を食べてしまうというシステムが基本になっています。 病原体を食べた食細胞は、TLR(トル様受容体)などのパターン認識受容体で、病原体や危険シグナルに共通するパターンを認識して活性化します。 一方、「獲得免疫」は「抗原」というターゲットに対して対応する免疫応答です。この獲得免疫は、自然免疫による病原体認識という段階を経なければ始動しないことが判っています。 その理由は、抗原特異的なT細胞が活性化するには、樹状細胞から抗原提示を受けなければならないのですが、樹状細胞は他の食細胞と同様にパターン認識受容体で病原体やがん細胞を認識して活性化する必要があるからです。
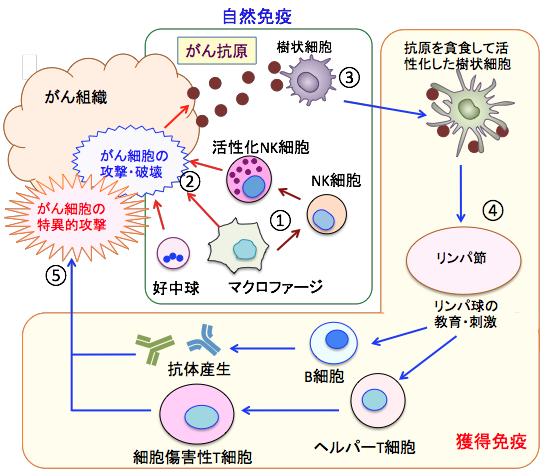
①活性化したマクロファージはナチュラルキラー細胞(NK細胞)を活性化する。②活性化されたマクロファージやNK細胞などががん細胞を攻撃してがん細胞の破壊が起こるとがん抗原が樹状細胞に取込まれる。抗原による感作の必要のないがん細胞に対する第一次防衛機構が「自然免疫」となる。④がん抗原を貪食した樹状細胞はがん抗原の情報をT細胞やB細胞に渡して活性化する。⑤がん抗原特異的な免疫応答によるがん細胞の攻撃が「獲得免疫」となる。
【獲得免疫の始動には樹状細胞の活性化が必要】
樹状細胞(Dendritic cell)は,細胞表面に突起構造を持っていることから名付けられ,高い運動性を有する免疫細胞の一種で,身体のあらゆる場所に存在しています。哺乳動物の免疫系では,最も強力な抗原提示細胞として機能しています。
末梢で病原体やがん細胞を食べて活性化した樹状細胞は最寄りのリンパ節に移動します。樹状細胞は取り込んだ細胞を細胞内で分解してペプチド(アミノ酸が数個つながったもの)にし、これらのペプチドはMHCという分子と結合して細胞表面に提示されます。 樹状細胞は活性化する前も「MHC+ペプチド」が提示されていますが、活性化されると、樹状の突起をめいっぱいに出して表面積を広げ、できるだけ多くの抗原を提示しようとします。 樹状細胞が提示する抗原と反応するヘルパーT細胞(CD4+)やキラーT細胞(CD8+)が活性化されて、リンパ球による抗原特異的な免疫応答が活性化されます。
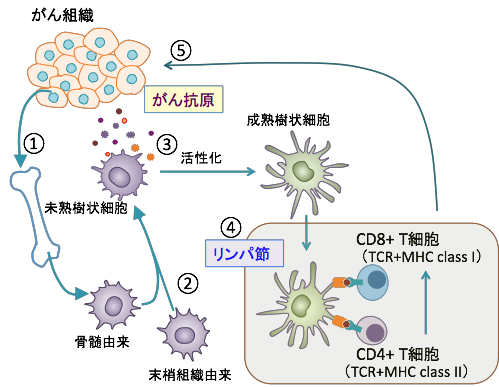
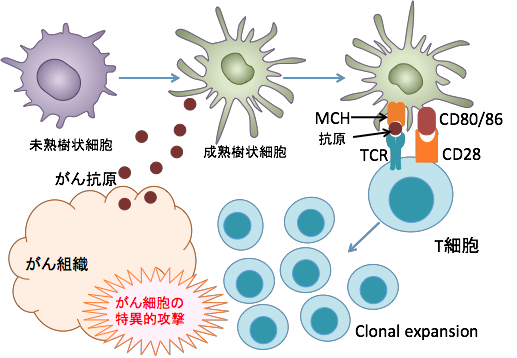
①腫瘍由来因子が未成熟な樹状細胞を骨髄から動員する。②末梢組織からも未熟樹状細胞が腫瘍組織に集まってくる。③死滅したがん細胞から放出されたがん抗原は未熟樹状細胞に取り込まれ、活性化されて成熟樹状細胞に分化誘導される。④成熟樹状細胞はリンパ節に移動し、MHCクラスI及びクラスIIに結合したがん抗原をTCR(T細胞受容体)を介して、CD4+T細胞(ヘルパーT細胞)とCD8+T細胞(キラーT細胞)に提示する。⑤抗原提示をうけて活性化したキラーT細胞はがん抗原特異的な免疫学的攻撃を行う。
【トル様受容体が自然免疫を発動させる】
生体は「自己にない分子パターンを認識する」というメカニズムで細菌やウイルスや真菌などの病原体を認識して、自然免疫を発動させます。 また、細胞傷害に伴って放出される細胞内分子を「危険シグナル(danger signals)」として認識し、自然免疫や炎症を発動させます。
このような自然免疫の発動で重要な役割を果たしているのがトル様受容体(Toll-like Receptor: TLR)です。 トル様受容体(TLR)は動物の細胞表面やエンドソームにある受容体タンパク質です。
TLRは、細菌やウイルスや原虫や真菌などに共通して保存されている病原体関連分子パターン(pathogen-associated molecular patterns)を認識します。
細胞がダメージを受けたとき、通常であれば細胞内に隠れている細胞内成分が放出され、炎症細胞や免疫細胞を活性化します。このような炎症を引き起こす細胞内成分をダメージ関連分子パターン(damage-associated molecular patterns;DAMPs)と総称しています。 DAMPsは細胞傷害に伴って細胞から放出され、周囲の組織や細胞に危険を知らせるアラームのような役割を担う因子のことです。 DAMPsが細胞外や細胞膜上に露出するような細胞死が起こると、炎症反応が引き起こされ、ダメージを受けた組織の修復が起こります。DAMPsもトル様受容体を介して自然免疫を始動させます。
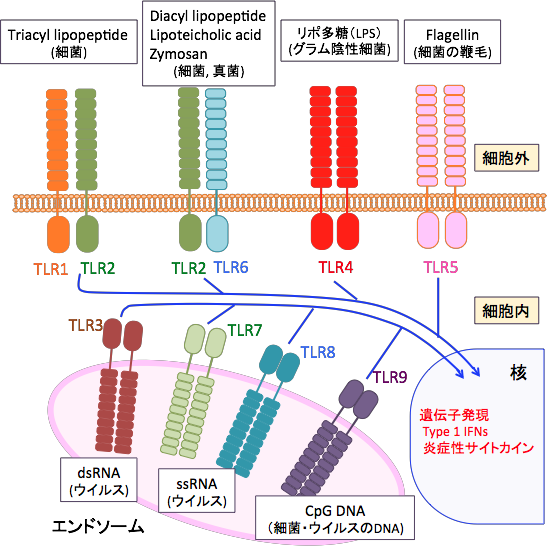
トル様受容体が認識する成分として、細菌表面のリポ多糖(LPS)、リポタンパク質、鞭毛のフラジェリン、ウイルスの一本鎖RNAと二本鎖RNA、細菌やウイルスのDNAに含まれる非メチル化CpGアイランドなどがあります。ある特定の分子を認識するのではなく、一群の分子を認識するパターン認識受容体です。 これらの受容体にリガンドが結合すると、そのシグナルによって自然免疫の応答が発動されます。
細菌やウイルス由来のリポ多糖、脂質、タンパク質を認識する TLR1,2,4,5,6はいずれも 細胞表面に存在し、細胞表面で微生物の表層成分を認識しシグナルを伝達する.一方,核酸を認識する TLR3,7,8,9はいずれもエンドソーム(エンドサイトーシスによって細胞内へと取り込まれた様々な物質の選別・分解・再利用などを制御する細胞内小器官)などの細胞内オルガネラ膜に局在し、エンドソームでリガンドを認識しシグナルを伝達する。(参考:Immunotherapy. 2009;1(6):949-964.のFig1)
【抗原提示とT細胞の活性化】
病原微生物の侵入など何らかの原因で炎症が起こると、血管から顆粒球や単球などが遊走して来ます。このように炎症反応によって集まってきたり、あるいは組織に常在していた樹状細胞やマクロファージは、侵入した細菌やウイルス粒子、あるいは死滅した細胞の死骸や断片などを取り込み、リンパ液の流れに沿って所属リンパ節に移動します。
樹状細胞やマクロファージは取り込んだタンパク質を分解し、その結果産生されたペプチド(アミノ酸が数個から数十個つながったもの)をMHC(major histocompatibility complex:主要組織適合抗原複合体)分子の上に提示します。
活性化した樹状細胞はリンパ節で手当たりしだいにナイーブT細胞(まだ一度も活性化されたことのないT細胞)とくっつきあって、何かを確かめます。ナイーブT細胞はその表面にT細胞抗原認識受容体(TCR)を持っています。樹状細胞の表面に提示されたMHC+抗原ペプチドとピタッとくっつく受容体(TCR)をもったナイーブT細胞と出会うと、そのT細胞を活性化します。
抗原を提示して活性化している樹状細胞にはCD80/86という補助刺激因子が発現しており、T細胞のCD28と結合し、刺激を送ります。 さらに、活性化した樹状細胞はサイトカインを放出しており、ナイーブT細胞はそれを浴びることになります。
このように①TCRを介するシグナルと②CD28を介する補助刺激と③サイトカインによる刺激を同時に受けたTリンパ球は初めて活性化し、TCRの特異性を保ったままで分裂・増殖して自らのクローンを増やします。 CD4陽性T細胞(ヘルパーT細胞)は、Th1またはTh2のパターンを示すサイトカイン産生細胞へと分化します。 CD8陽性T細胞(キラーT細胞)は成熟し、細胞質内にパーフォリンやグランザイムなどを含んだ細胞傷害顆粒を持つエフェクター細胞になります。
エフェクター細胞はリンパ節を離れ、胸管を経て循環血液中へと流れ込み、血流に従って全身を巡ります。炎症の起こっている組織から産生されるサイトカインやケモカインなどの作用でエフェクターT細胞は炎症部位に集まり、病原菌やがん細胞の攻撃に参加します。
がん細胞から放出されたがん抗原を未熟樹状細胞が取り込んで成熟して抗原を提示するとき、MCH(major histocompatibility complex:主要組織適合抗原複合体)分子にペプチド抗原を載せて細胞傷害性T細胞やヘルパーT細胞に提示する。このとき、MCH+ペプチド抗原にぴったり結合するTCR(T細胞受容体)を持つT細胞は、補助刺激因子(CD28とCD80/86など)や樹状細胞から放出されるサイトカインの働きで活性化され、がん抗原を認識するT細胞が増殖し、がん細胞を攻撃する。
【イミキモド(imiquimod)はTLR7のリガンド】
トル様受容体(TLR)シグナル系は自然免疫と獲得免疫の両方を活性化します。TLRの活性化はI型インターフェロンと炎症性サイトカインの遺伝子発現を促進します。 I型インターフェロンとはインターフェロンファミリーのうち、インターフェロンα(IFN-α)とインターフェロンβ(IFN-β)などを含めた総称で、ウイルス感染で誘導される抗ウイルス作用をもつサイトカインです。免疫系細胞から分泌されてマクロファージを活性化するインターフェロンγ(IFN-γ)はII型インターフェロンと言います。
I型インターフェロンは抗原提示、T細胞増殖、樹状細胞の成熟、ナチュラルキラー細胞の活性化を促進します。
トル様受容体(TLR)を介する樹状細胞の活性化は、貪食作用、成熟、流域リンパ節への移動、Th1サイトカインの分泌、リンパ球への抗原提示能を亢進します。
TLRのアゴニストはがんの免疫療法において有望な治療薬となりうると考えられており、多くの物質が臨床使用に向けて開発中です。 腫瘍局所にTLRアゴニストを投与すると、自然免疫と獲得免疫を誘導し、さらに腫瘍の微小環境に様々な作用を及ぼして、腫瘍を効率的に排除することができます。
TLRアゴニストは樹状細胞を活性化し、T細胞応答を増強し、制御性T細胞の免疫抑制作用を減弱させるので、がんワクチン療法の効果を増強します。 抗がん剤治療や放射線治療や抗体療法や分子標的薬とTLRアゴニストとの併用療法に関する研究が進行中です。 すでに臨床で使用されているものもあります。BCGやピシバニールはTLRを活性化します。さらにTLR7のリガンドのイミキモド(imiquimod)という塗り薬が、尖圭コンジロームや皮膚がんの治療に使用されています。
イミキモド(Imiquimod)は合成イミダゾキノリン(imidazoquinoline)で、樹状細胞やマクロファージなどに発現しているTLR7(Toll-like receptor 7)にリガンドとして直接結合し、シグナルを伝えることによって、I型インターフェロンを誘導し自然免疫を活性化します。
TLRはパターン認識受容体で、病原体の侵入を感知して自然免疫を活性化し、ついで獲得免疫を作動させます。TLR7は樹状細胞やマクロファージなどの抗原提示細胞のエンドソームの膜に存在し、ウイルスの一本鎖RNAがリガンドになります。 TLR7の活性化はIFN-α、IL-12、TNF-αなどの炎症性サイトカインの産生を増やし、樹状細胞の成熟と抗原提示能を促進します。
欧米では塗布薬(5% imiquimodクリーム)として販売され、基底細胞がんや尖圭コンジローマに対して使用され、さらに日光角化症、ボーエン病など表在性の皮膚悪性腫瘍でも有効性が認められています。
欧米で実施された基底細胞がん(BCC)を対象にした臨床試験では、表在型BCCに対し6週間毎日または5回/週の外用で、80%前後の腫瘍の病理学的消失率が認められています。 有害事象としては紅斑、びらん、潰瘍、局所刺激感などの局所反応が主体であり、おおむね安全に使用できます。
このような皮膚がんに対する効果は、イミキモドがTLR7のアゴニストで、自然免疫を活性化して、皮膚がんに対する特異免疫を誘導して、免疫機序で腫瘍を縮小・消滅させると考えられています。
したがって、皮膚がん以外の転移性皮膚腫瘍に対しても効果が期待でき、さらには、皮膚投与でイミキモドが腫瘍近くのリンパ節に取り込ませることも可能なので、皮膚転移以外の全身のがん転移にも効果があります。
実際に乳がんの皮膚転移にイミキモドクリームが有効であった症例の報告があります。さらに、イミキモドクリームの皮膚投与は頭蓋内腫瘍を縮小させたり、肺組織の免疫を高めるなどの動物実験の結果が報告されています。
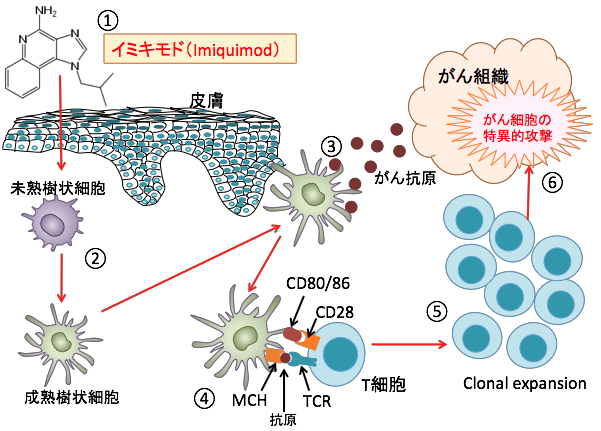
①トル様受容体7(TLR7)のリガンドであるイミキモドを皮膚に塗布すると皮下に吸収され、②皮下の未熟樹状細胞を成熟させる。③がん組織から放出されるがん抗原を成熟樹状細胞が取り込むと活性化され、T細胞に抗原提示を行う。④樹状細胞はMCH分子の上にがん抗原を乗せ、この抗原にぴったり合うT細胞受容体(TCR)を見つけると、補助刺激因子(CD28とCD80/86など)の結合やサイトカインの放出などによって、がん抗原を認識するT細胞が活性化される。⑤その結果、がん抗原を認識するTCRをもつT細胞がクローナルに増殖する。⑥抗原特異的に活性化されたT細胞はがん細胞を攻撃する。
【ピドチモド(Pidotimod)は樹状細胞の成熟を促進する】
ピドチモド(Pidotimod)は、2つのアミノ酸が結合したようなジペプチド様構造の生体応答調節療剤(Biological Response Modifiers)の一種です。自然免疫と獲得免疫の両方を活性化する効果が知られており、感染症の予防や治療に有効であることが複数の臨床試験で明らかになっています。
例えば、上気道感染症や尿路感染症を頻回に繰り返す小児を対象にした臨床試験で、ピドチモドは感染症の発症頻度を減少させる効果が確認されています。ピドチモドの免疫増強効果は老化やダウン症候群やがんのような免疫低下を起こしやすい状況でより高い効果が認められています。
ピドチモドの免疫刺激作用のメカニズムとして、樹状細胞の成熟を促進し(HLA-DRと補助刺激分子の発現亢進)、樹状細胞からの炎症性サイトカインの産生を刺激してT細胞の増殖とTh1フェノタイプへの分化誘導、ナチュラルキラー細胞(NK細胞)の機能亢進と貪食能の亢進などが報告されています。
ピドチモドはインターロイキン-12(IL-12)の産生を高める効果があります。IL-12は当初「NK細胞刺激因子」の名称で報告されたように、NK細胞に対する著明な活性化作用を特徴とするサイトカインです。IL-12はT細胞やNK細胞に対して細胞増殖の促進、細胞傷害活性誘導、IFN-γ産生誘導、LAK細胞誘導などの作用を示します。 このように、ピドチモドは自然免疫と獲得免疫の両方を活性化し増強します。
ピドチモドは1日400〜800mg程度を1日1〜2回に分けて服用します。 経口摂取での生体利用率(bio-availability)は42〜44%で、血中の半減期は約4時間です。体内では代謝されずにそのままの形で尿中から排泄されます。 幾つかの国(イタリア、ギリシャ、中国、ベトナム、コスタリカ、ドミニカ共和国、エルサルバドル、グアテマラ、ホンジュラス、メキシコ、パナマ)で医薬品として販売されています。
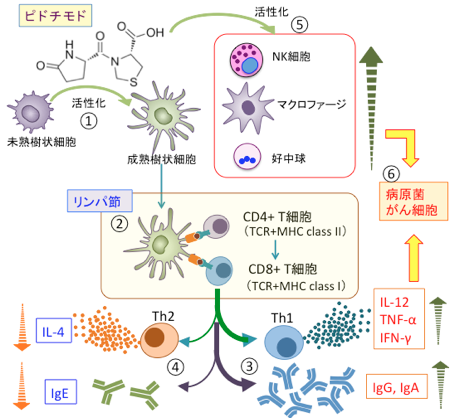
①ピドチモドは未熟樹状細胞を活性化して成熟樹状細胞に分化させる。②成熟樹状細胞はリンパ節に移動し、CD4+T細胞(ヘルパーT細胞)とCD8+T細胞(キラーT細胞)に抗原提示によって活性化する。③リンパ球のTh1フェノタイプを促進してIL-12, TNF-α,インターフェロン-γ(IFN-γ) の産生を亢進し、B細胞からIgGと分泌型IgAの産生を亢進する。④一方、Th2フェノタイプを抑制して抗アレルギー作用を示す。⑤ピドチモドはNK細胞、マクロファージ、好中球など自然免疫も活性化する。⑥これらの総合作用によって感染症やがんに対する免疫力を増強する。
【IL-12産生を刺激しPGE2の産生を抑制するとTh1細胞活性が増強する】
T細胞(Tリンパ球)には、細胞表面にCD4という分子を出しているヘルパーT細胞(CD4陽性T細胞)と、CD8という分子を出しているキラーT細胞(CD8陽性T細胞)があります。まだ抗原に出会ったことのないT細胞をナイーブT細胞と言います。 樹状細胞やマクロファージなどの抗原提示細胞が抗原提示を行う相手はナイーブT細胞です。 抗原提示細胞が提示する抗原にぴったり結合する受容体をもったT細胞が活性化されます。これを抗原特異的な活性化と言います。抗原提示を受けて活性化したT細胞は増殖し、抗原特異的な免疫応答を開始します。
ヘルパーT細胞にはTh1細胞(細胞性免疫)とTh2細胞(液性免疫)があります。抗原提示細胞がIL-12を産生するか、それともプロスタグランジンE2(PGE2)を産生するかがTh1とTh2のどちらが優位になるかを決定しています。 すなわち、ナイーブヘルパーT細胞(Th0)は抗原提示細胞が産生するサイトカインによって細胞性免疫に関与するTh1細胞か、液性免疫に関与するTh2細胞へと分化します。
抗原提示細胞が抗原をナイーブT細胞に提示する際にIL-12を分泌するとTh1細胞(T helper 1 cell)に分化します。Th1細胞はIFN-γ、IL-2、TNF-αなどのサントカインを産生し、細胞性免疫を促進します。Th1細胞が産生するIFN-γはTh0細胞(ナイーブヘルパーT細胞)のTh1細胞への分化を促進します。
一方、抗原提示細胞が抗原をナイーブT細胞に提示する際にプロスタグランジンE2(PGE2)を分泌するとTh2細胞(T helper 2 cell)に分化します。Th2細胞はIL-4、IL-5、IL-10などのサイトカインを産生し、液性免疫(抗体産生)を促進します。Th2細胞が産生するIL-4はTh0細胞(ナイーブヘルパーT細胞)のTh2細胞への分化を促進します。
がん細胞を攻撃する抗腫瘍免疫を高めるためにはTh1細胞を増やして細胞性免疫を高める必要があります。そのためには、抗原提示細胞からのIL-12産生を促進し、PGE2の産生を抑制することがポイントになります。
ピドチモドは樹状細胞の成熟とIL-12の産生を促進し、Th1細胞を増やします。PGE2産生はシクロオキシゲナーゼ-2(COX-2)の阻害剤のcelecoxib(商品名:セレコックス)で阻止できます。
実際の多くの実験系で、がんワクチンや樹状細胞療法にCOX-2阻害剤のcelecoxibを併用すると抗腫瘍免疫が増強することが示されています。 つまり、ピドチモドとセレコックスの併用はTh1細胞を増やして細胞性免疫を高める方法となります。(下図)
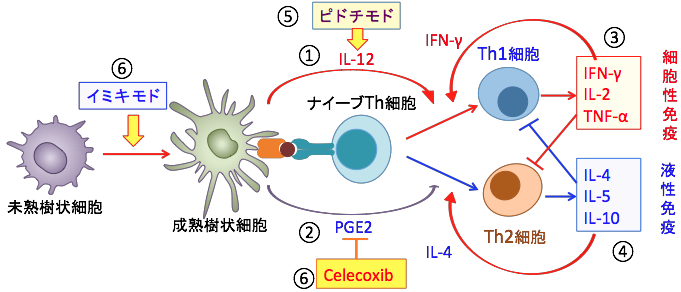
①ナイーブヘルパーT(Th)細胞が抗原提示細胞(樹状細胞やマクロファージ)から抗原の提示を受ける際、IL-12はTh1細胞への分化を促進する。②一方、プロスタグランジンE2(PGE2)はTh2細胞への分化を誘導する。③Th1細胞はインターフェロン-γ(IFN-γ)、IL-2、TNF-αなどのサイトカインを産生し、細胞性免疫を促進する。IFN-γはナイーブTh細胞のTh1細胞への分化を促進する。④Th2細胞はIL-4、IL-5、IL-10などのサイトカインを産生して液性免疫(抗体産生)を促進する。IL-4はナイーブTh細胞のTh2細胞への分化を促進する。⑤ピドチモドは樹状細胞からのIL-12の産生を亢進し、⑥COX-2阻害剤のcelecoxibはPGE2の産生を阻害するので、両者を併用するとTh1細胞への分化を促進して抗腫瘍免疫を亢進できる。⑥さらに、イミキモドはトル様受容体7(TLR7)を刺激して樹状細胞の成熟を促進する。したがって、ピドチモド、セレコックス、イミキモドの3種を併用するとがん細胞に対する免疫的排除を促進できる。
【シメチジンは骨髄由来抑制細胞を阻害する】
多くのがん患者において、末梢血中の骨髄由来抑制細胞(MDSC)が増えており、MDSCの数が多いほど予後が悪いという報告があります。 肥満細胞からのヒスタミンがMDSCの移動や増殖を促進することが報告されています。 肥満細胞の働きを阻害してヒスタミンの分泌を抑制したり、ヒスタミン受容体の阻害剤が骨髄由来抑制細胞の働きを抑制して、抗腫瘍免疫を高める作用が報告されています。
ヒスタミン受容体拮抗薬のシメチジンには様々な抗腫瘍効果が報告されていますが、抗腫瘍免疫を高める作用があり、そのメカニズムの一つとして骨髄由来抑制細胞の抑制作用が報告されています。
生体内アミンであるヒスタミンは、炎症反応や胃酸分泌、アレルギー反応など様々な生理反応に関与しています。 ヒスタミンは細胞表面にある受容体に結合することによって細胞にヒスタミンの刺激を伝えます。 ヒスタミンの受容体は現在までに 3 種類のサブタイプ(H1~H3)が見つかっていますが、そのうち H2 受容体は胃酸分泌において中心的な役割を担っており、その拮抗薬であるシメチジンは胃酸の分泌を抑える効果により胃炎や消化性潰瘍や逆流性食道炎などの治療薬として使用されています。
1980 年代後半に デンマークのTonnesen らにより、シメチジンが胃がん患者に対し延命効果を示すことが報告され、その後、大腸がん、悪性黒色腫に対しても同様の効果を示すことが報告されています。
例えば、治癒切除術後5-FU(200mg/日)投与を受けている原発性大腸がん患者(シメチジン800mg/日併用群34例、非併用群30例の計64例)において、平均10.7年の観察期間での10年生存率は、シメチジン併用群で84.6%、シメチジン非併用群で49.8%でした(P<00001)。 切除手術を受けた大腸がん患者を対象にした臨床試験のメタ解析によると、シメチジンを服用することによって死亡リスクが0.53に低下すると報告されています。
ヒスタミンにはがん細胞の増殖を促進する作用や、細胞性免疫を抑制するリンパ球(骨髄由来抑制細胞や制御性T細胞)を活性化することなどが報告されており、そのためシメチジンの延命効果は、がん細胞に対するヒスタミンの細胞増殖促進作用を阻害する機序や、がん細胞に対する免疫力を活性化させ る可能性などが指摘されています。
さらに近年では、シメチジンが接着因子 E-セレクチンの発現を抑 制することによりがんの転移を抑制する抑える機序や、インターロイキン 12の発現上昇を介したナチュラルキラー細胞活性化、血管新生阻害作用によって腫瘍組織の増大を阻止する可能性、がん細胞にアポトーシス(細胞死)を誘導する作用など、新たなメカニズムも報告されています。
【シメチジンは様々なメカニズムで抗腫瘍免疫を高める】
シメチジンには様々なメカニズムで抗腫瘍免疫を増強することが報告されています。以下のような作用機序が報告されています。
○ 抗腫瘍免疫(Th1)の増強:
生体の免疫機構は細胞性免疫型(Th1)と体液性免疫型(Th2)のバランスにより制御されていますが、多くのがん患者や担がん状態の実験動物においてその免疫機構が Th2 型へ移行していることが報告されています。 がん細胞の排除には細胞性免疫(Th1細胞)が中心的な役割を担うと考えられていることから、Th2 型への移行は担がん宿主の免疫機能低下の一因であると考えられています。
免疫機構が Th2 型に移行している担がんマウスに IL-12 を投与すると腫瘍の顕著な退縮が認められることが数多く報告されています。 IL-12 はナチュラルキラー細胞や T 細胞をその傷害活性の誘導・増強に向けて活性化するのみでな く、生体の細胞性免疫を促進する根源的な役割を担うサイトカインです。 IL-12 の主な産生細胞 はマクロファージおよび B 細胞であることが知られていますが、近年マクロファージからの IL-12 産生をヒスタミンが抑制すること、またその抑制作用はヒスタミン H2 受容体拮抗薬を前処置した際には認められないことが報告されています。
多くのがん組織においてはヒスタミン含量の上昇や、ヒスタミン合成酵素であるヒスチジンデカルボキシラーゼ活性の上昇が確認されています。これらのことは、担がん状態における免疫機構の Th2 型への移行原因の一つに、上昇したヒスタミンに よるマクロファージからの IL-12 産生抑制が関与している可能性を示唆するものです。
したがって、ヒスタミンH2受容体拮抗薬は、IL-12の産生を高め、細胞性免疫(Th1細胞)の活性を高める効果が期待できます。○ 樹状細胞の活性化:
がん細胞に対する免疫応答の中でがん抗原に対する免疫応答誘導において鍵となる細胞である樹状細胞の抗原提示能を増強させる可能性が報告されています。○ ナチュラルキラー細胞の活性化:
インターロイキン12(IL-12)の発現を亢進してナチュラルキラー細胞活性を高める効果が報告されています。インターロイキン-12(IL-12)は、当初"NK細胞刺激因子"の名称で報告されたように、NK細胞に対する著明な活性化作用を特徴とするサイトカインです。 IL-12はB細胞および単球系細胞より産生され、T細胞やNK細胞に対して細胞増殖の促進、細胞傷害活性誘導、IFN-γ産生誘導、LAK細胞誘導などの作用を示します。こうした細胞性免疫機能への作用から、IL-12には感染防御やがん治療や免疫不全症の改善における臨床応用が期待されています。 前述のごとく、ヒスタミンはIL-12 の産生を抑制するので、シメチジンはIL-12の産生を高めてナチュラルキラー細胞活性を高める効果を発揮します。○ 細胞傷害性Tリンパ球の活性化:
ヒスタミンには細胞傷害性Tリンパ球の生成を抑制する作用が知られています。さらにヒスタミンH2受容体はサプレッサーT細胞にも発現が認められ、ヒスタミンによりサプレッサーT細胞が活性化され、宿主側の免疫システムを減弱させると報告されています。そこでヒスタミンH2受容体拮抗薬が上記のヒスタミンの作用を抑制し、免疫システムを増強し、抗腫瘍作用を示すのではないかと推測されています。 また、抗腫瘍免疫の働きを弱める骨髄由来抑制細胞や制御性T細胞の働きをヒスタミンが高めるので、抗腫瘍免疫が抑制されるという報告もあります。
シメチジン投与群では腫瘍組織にリンパ球の浸潤が多く見られたという報告があります。このような腫瘍組織に浸潤するリンパ球の存在は、腫瘍に対する宿主の免疫応答を意味しており、予後が良いことを示すサインと言えます。つまり、シメチジンはがん組織に対する免疫応答(細胞性免疫)を増強する効果があると言えます。
大腸がんはヒスタミンを分泌し、がん組織の中のヒスタミンのレベルが高いことが報告されています。つまり、がん患者や手術後の病態における免疫抑制には、ヒスタミンが関与している可能性があり、H2ブロッカーによって、免疫力低下の機序を解除できる可能性が指摘されています。
【がん患者のTh1サイトカイン産生を高める漢方薬】
リンパ球にはB細胞・T細胞・ナチュラルキラー(Natural killer, NK)細胞などがあります。 B細胞は抗体という飛び道具を使って細菌やウイルスを攻撃するもので、これを「液性免疫」といいます。IgEという抗体の一種が関与するアレルギー性疾患はこの液性免疫が過剰に反応する結果発生します。
一方、ウイルス感染細胞やがん細胞など自分の細胞に隠れている異常を発見して、Tリンパ球やNK細胞などが直接攻撃する免疫の仕組みを「細胞性免疫」といいます。細胞性免疫はがんに対する生体防御に重要な役割を果たしますが、調節が狂って正常な自分の細胞を攻撃すると様々な自己免疫疾患の発病に関連します。
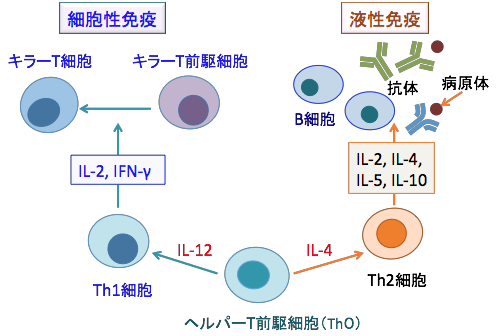
この液性免疫と細胞性免疫の制御は2種類のヘルパーT細胞 (Th) のバランスによって決まります。ヘルパーT細胞は、B細胞やT細胞の増殖や働きを調節するタンパク質(サイトカイン)を分泌して、液性免疫と細胞性免疫のバランスを調節しており、そのサイトカインの産生パターンから、Th1(1型ヘルパーT) 細胞とTh2(2型ヘルパーT) 細胞に分類されます。 Th1細胞はインターフェロン・ガンマ(IFN-γ)や インターロイキン-2(IL-2)を分泌して細胞性免疫に関与し、Th2細胞はIL-4, IL-5, IL-6, IL-10などを分泌して液性免疫に関与します。
ヘルパーT前駆細胞(Th0)がTh1細胞になるためにはマクロファージや樹状細胞から分泌されるIL-12が必要であり、一方、Th2細胞となるためにはT細胞から分泌されるIL-4が必要とされています。
ヘルパーT前駆細胞(Th0)は1型ヘルパーT細胞(Th1)と2型ヘルパーT細胞(Th2)に分化誘導される。 Th1細胞はインターフェロン・ガンマ(IFN-γ)や インターロイキン-2(IL-2)を分泌して細胞性免疫に関与し、Th2細胞はIL-4, IL-5, IL-6, IL-10などを分泌して液性免疫に関与する。ヘルパーT前駆細胞(Th0)がTh1細胞になるためにはマクロファージや樹状細胞から分泌されるIL-12が必要であり、一方、Th2細胞となるためにはT細胞から分泌されるIL-4が必要とされている。がん細胞を攻撃するのはTh1細胞である。
漢方薬の補剤といわれる処方はTh1細胞を活性化して細胞性免疫を増強することが知られています。例えば、体力や免疫力を高める漢方処方の代表である補中益気湯(ほちゅうえっきとう)や十全大補湯(じゅうぜんたいほとう)はTh1細胞を活性化して細胞性免疫を高めることが報告されています。
がん患者ではTh2サイトカインが優位になっており、このTh2サイトカインの優位性が腫瘍の進展と関連していることが知られています。 したがって、がん患者におけるTh2優位性の状態を逆転することは、がん治療において有用であると考えられています。
漢方薬に使用される黄耆(おうぎ)と川芎(せんきゅう)が、がん患者におけるTh2サイトカイン優位な免疫状態をTh1サイトカイン優位に逆転する効果を示す研究結果が報告されています。また、紅参(こうじん)もTh1サイトカインを誘導します。
栄養不全・加齢・ストレスや慢性消耗性疾患などでは、TH1が低下しTh2優位となります。このような状態では、がん細胞に対する免疫(腫瘍免疫)の働きは低下した状態になります。がん治療で用いられる免疫増強剤の多くは、T細胞をTh1タイプが優位になるように働いて細胞性免疫を高めます。しかし、栄養状態や体力の低下などTh1活性を低下させる要因が強いときには、これらを改善しないと、いくら免疫増強剤を投与しても十分な効果を発揮できません。
また、がん細胞が作り出す有害物質によって、がんを持った体の代謝機構や防御機構が乱され、栄養素の消化・吸収・利用が障害されて、食欲不振や体重減少が引き起こされます。さらに体が消耗状態に陥ると、老廃物が蓄積し、栄養物質の供給は障害されます。このようながん患者にみられる血液や体液が汚れた状態を悪液質といいます。悪液質の状態ではTh2が優位となってTh1の活性を阻害する方向に働いているため、どんな免疫療法を試みてもその効果が現われにくくなっています。そのような状況に対しては、組織の循環や新陳代謝を改善し、栄養状態を高めることによって悪液質を改善すれば、Th2優位の状態から脱することができます。
例えば、人参にはがん患者における食欲不振や体重減少を改善し、悪液質の改善にも効果があることが報告されています。 したがって、十全大補湯のような補剤や、血液循環や新陳代謝を良くする駆瘀血薬や、炎症やがん性悪液質を改善する清熱解毒薬などを組み合わせることによって、より有効にTh1優位の抗腫瘍免疫を増強できます。
【免疫抑制のメカニズムを解除すれば抗腫瘍免疫が高める】
体内では免疫細胞ががん細胞を認識して攻撃しています。腫瘍組織にCD8陽性T細胞(キラーT細胞)が多く集まっている場合は予後が良いという報告もあります。 そこで、樹状細胞の成熟を促進し、ヘルパーT細胞のTh1細胞への分化を誘導し、がん抗原特異的なキラーT細胞を増やすことができれば、がん細胞を死滅させる効果が得られます。 これが樹状細胞療法やがんワクチン療法の原理です。
例えば、体内から採取した樹状細胞とがん細胞を混ぜて培養し、樹状細胞ががん抗原を提示できるようにして体内に戻すという治療が行われています。 体外で培養しなくても、腫瘍組織でがん細胞が免疫原性細胞死を起こしている状態に、樹状細胞の成熟やヘルパーT細胞のTh1細胞への分化や、キラーT細胞の増殖を促進すれば、がん組織を免疫細胞が攻撃してくれるはずです。
しかし、多くの場合、このような免疫療法はあまり効果が得られていません。その理由の一つが、骨髄由来抑制細胞(myeloid-derived suppressor cell)や制御性T細胞(Treg)などの免疫抑制性細胞の存在や、PD-1/PD-L1やCTLA-4による免疫細胞の活性抑制のメカニズムの存在です。
そこで、このような免疫抑制性のメカニズムを阻止すれば、免疫療法の効き目を高めることができます。 前述のようにCOX-2阻害剤のcelecoxib(商品目:セレコックス)とピドチモドの併用は樹状細胞の成熟とTh1細胞の分化とCTL(細胞傷害性T細胞)の活性を高めて、抗腫瘍免疫を亢進します。
さらに骨髄由来抑制細胞(MDSC)の働きを抑制するシメチジン、MDSCを分化誘導して免疫抑制活性を低下させるレチノイドとビタミンD3の併用も免疫療法の効き目を高めます。 低用量のシクロフォスファミド(エンドキサン)の投与がMDSCを死滅させて抗腫瘍免疫を高めることが報告されています。 さらに、紅参(こうじん)、黄耆(おうぎ)、川芎(せんきゅう)などTh1サイトカインの産生を高める漢方治療を併用すると、がん細胞に対する免疫細胞の攻撃力を増強できると思います。
このように「腫瘍組織における免疫抑制性の微小環境」を改善する治療法は、がんの免疫療法の効果を高めることができます。
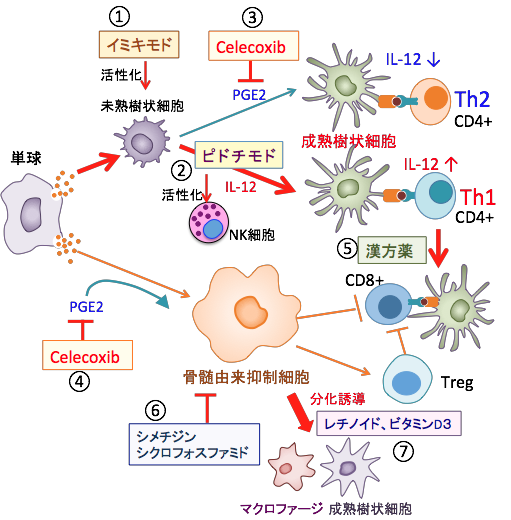 |
①イミキモドはトル様受容体TLR7を刺激して未熟樹状細胞の成熟・活性化を促進する。②ピドチモドは樹状細胞の成熟とIL-12産生を促進して1型ヘルパーT細胞(Th1)を増やし、ナチュラルキラー細胞(NK細胞)を活性化する。③プロスタグランジンE2(PGE2)はIL-12の産生を抑制して2型ヘルパーT細胞(Th2)への分化を誘導するので、COX-2阻害剤のCelecoxibはPGE2の産生を阻害してTh2への分化誘導を阻止する。④PGE2は骨髄由来抑制細胞(MDSC)の増殖を促進するので、CelecoxibはMDSCの増殖を阻止する。⑤漢方薬(紅参、黄耆、川芎など)はTh1サイトカインの産生を高めて細胞性免疫を活性化する。⑥シメチジンとシクロフォスファミドはMDSCの活性や生存を阻害する。⑦レチノイドとビタミンD3は未熟なMDSCを成熟させ分化誘導によって免疫抑制活性を低下させる。 |
|---|